ความ เข้มข้น ของ สารละลาย Ppt
24 g และ น้ำ 100 g สารละลายมีความเข้มข้นเท่าใดในหน่วยส่วนในล้านส่วน 15 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 7 ถ้าในอากาศ 100 cm3 มี N2O 3. 3 x 10-5 cm3 ความเข้มข้นของ N2O ในหน่วย ppb มีค่าเป็นเท่าใด 16 ความเข้มข้นของสารละลาย (3) โมลาริตี หรือเรียกอีกอย่างหนึ่งว่าความเข้มข้นเป็นโมลาร์ ใช้สัญลักษณ์ M หมายถึงจำนวนโมลของตัวละลายที่ละลายในสารละลาย 1 ลูกบาศก์เดซิเมตร หรือ 1 ลิตร จึงมีหน่วยเป็นโมลต่อลูกบาศก์เดซิเมตร หรือโมลเป็นลิตร เช่น สารละลายกรดซัลฟิวริก เข้มข้น 1. 0 M หมายความว่า สารละลาย 1 ลูกบาศก์เดซิเมตรหรือ 1 ลิตร มีกรดซัลฟิวริกละลายอยู่ 1 โมล เขียนความสัมพันธ์ได้ดังนี้ 17 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 8 สารละลายที่ได้จากการละลาย NaOH จำนวน 15. 0 g ในน้ำ จนสารละลายมีปริมาตร 250 cm3 จะมีความเข้มข้นกี่โมลาร์ 18 19 20 ความเข้มข้นของสารละลาย (4) โมแลลิตี หรือเรียกย่อๆว่า โมแลล ใช้สัญลักษณ์ m หมายถึงจำนวนโมลของตัวละลายที่ละลายในตัวทำละลาย 1 กิโลกรัม มีหน่วยเป็นโมลต่อ 1 กิโลกรัม เช่น สารละลาย Na2CO3 0. 5 โมแลล หมายความว่ามี Na2CO3 0. 5 โมล ละลายในน้ำ 1 กิโลกรัม เขียนความสัมพันธ์ได้ดังนี้ 21 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 9 เมื่อละลายน้ำตาลทราย 34.
ความ เข้มข้น ของ สารละลาย pp.asp
1 ความเข้มข้นของสารละลายในหน่วยร้อยละโดยมวล ครูกนกวรรณ ศรชัย. mp4 1. 2 ร้อยละโดย ปริมาตร/ปริมาตร หรือร้อยละโดยปริมาตร สำหรับหน่วยนี้ นิยมใช้กับสารละลายที่เป็นของเหลวหรือแก๊ส ละลายในของเหลว เป็นหน่วยที่บอกให้ทราบว่ามีตัวทำละลายอยู่กี่หน่วยปริมาตร ในสารละลาย 100 หน่วยปริมาตรเดียวกัน ที่นิยมใช้คือ ลูกบาศก์เซนติเมตร เช่น น้ำส้มสายชูร้อยละ 5 โดยปริมาตร/ปริมาตร ปริมาตรตัวทำละลาย = ปริมาตรของสารละลาย - ปริมาตรของตัวถูกละลาย ปริมาตรน้ำ = ปริมาตร น้ำส้มสายชู - ปริมาตร กรดน้ำส้มสายชู = 100 - 5 = 95 ลบ. ซม. นั่นคือ สารละลายน้ำส้มสายชูร้อยละ 5 จะมีน้ำเป็นองค์ประกอบ(ตัวทำละลาย)อยู่ 95 ลูกบาศก์เซนติเมตร 1. 3 ร้อยละโดยมวลต่อ/ปริมาตร หรือร้อยละโดยปริมาตร สำหรับหน่วยนี้ นิยมใช้กับสารละลายที่เป็นของแข็ง ละลายในของเหลว เป็นหน่วยที่บอกให้ทราบว่า มีตัวทำละลายอยู่กี่หน่วยมวล ในสารละลาย 100 หน่วยปริมาตร เช่น สารละลายเกลือแกง (น้ำเกลือ) เข้มข้น 8% (ร้อยละ 8) โดยมวลต่อปริมาตร หมายถึง มีเกลือแกง 8 กรัมละลายอยุ่ในน้ำเกลือ 100 ลูกบาศก์เซนติเมตร ปริมาตรตัวทำละลาย = ปริมาตรของสารละลาย - มวลของตัวถูกละลาย น้ำ = น้ำเกลือ - เกลือ = 100 - 8 = 92 ลูกบาศก์เซนติเมตร นั่นคือ สารละลายเกลือแกงเข้มข้น 8% จะมีน้ำเป็นองค์ประกอบ(ตัวทำลาย) อยู่ 92 ลูกบาศก์เซนติเมตร 2. )
30 x 10-5 cm3 ความเข้มข้นเป็นร้อยละของ แก๊ส N2O ในอากาศมีค่าเท่าใด 7 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 3 สารละลาย NaOH เข้มข้นร้อยละ 6. 00 โดยมวล จำนวน 200 g มี NaOH อยู่ในสารละลายกี่กรัม 8 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 4 จงหาปริมาตรของสารละลาย Fe(NO3)3 เข้มข้นร้อยละ 15 โดยมวล ซึ่งมี Fe(NO3)3 ละลายอยู่ 30 g สารละลายมีความหนาแน่น g/cm3 ที่ 25oC 9 10 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 5 จงหามวลของ NiSO4 ในสารละลาย NiSO4 เข้มข้นร้อยละ โดยมวล จำนวน 50 cm3 กำหนดให้ สารละลายมีความหนาแน่นเท่ากับ 1. 06 g/cm3 ที่ 25oC 11 ความเข้มข้นของสารละลาย (2) ส่วนในล้านส่วน (parts per million ใช้อักษรย่อ ppm) และ ส่วนในพันล้านส่วน (parts per billion ใช้อักษรย่อ ppb) เป็นหน่วยที่บอกปริมาณตัวละลายเป็นมวลหรือปริมาตรที่ละลายในสารละลาย 1 ล้านหน่วย และ 1 พันล้านหน่วยตามลำดับ เช่น ในแหล่งน้ำแห่งหนึ่งมีสารตะกั่วปนเปื้อน 0. 1 ppm หมายความว่าน้ำในแหล่งน้ำนั้น 1 ล้านกรัมมีตะกั่วละลายอยู่ 0. 1 กรัม หรือในเนื้อปลามีสารปรอทปนเปื้อนอยู่ 1 ppb หมายความว่า ในเนื้อปลานั้น 1 พันล้านกรัม มีสารปรอทปนเปื้อนอยู่ 1 กรัม 12 ความเข้มข้นของสารละลาย ความเข้มข้นในหน่วยนี้เขียนความสัมพันธ์ได้ดังนี้ 13 ความเข้มข้นของสารละลาย ในกรณีที่สารละลายเจือจางมากมวลของตัวละลายมีค่าน้อยมาก เมื่อเทียบกับมวลของตัวทำละลาย ทำให้มวลของสารละลายมีค่าใกล้เคียงกับมวลของตัวทำละลายจนถือว่าเท่ากัน จึงเขียนความสัมพันธ์ได้ว่า 14 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 6 ในสารละลาย Hg(NO3)2 ซึ่งมี Hg(NO3)2 อยู่3.
- ความเข้มข้นของสารละลาย - สารละลาย
- ความ เข้มข้น ของ สารละลาย ppt karaoke
- (Review) ไอเท็มดี ไอเท็มร่วงของสาวผมสั้น (แต่อยากยาว)
- เพลง i just called to say i love you lirik
- รอก ตก ปลา เพ นางสาว
- ความเข้มข้นของสารละลาย - เรียนรู้วิทยาศาสตร์พื้นฐาน กับครูทวี
- ปาก มี กลิ่น ทํา ไง ดี
- ขาย เลนส์ fuji 55 200 มือ สอง
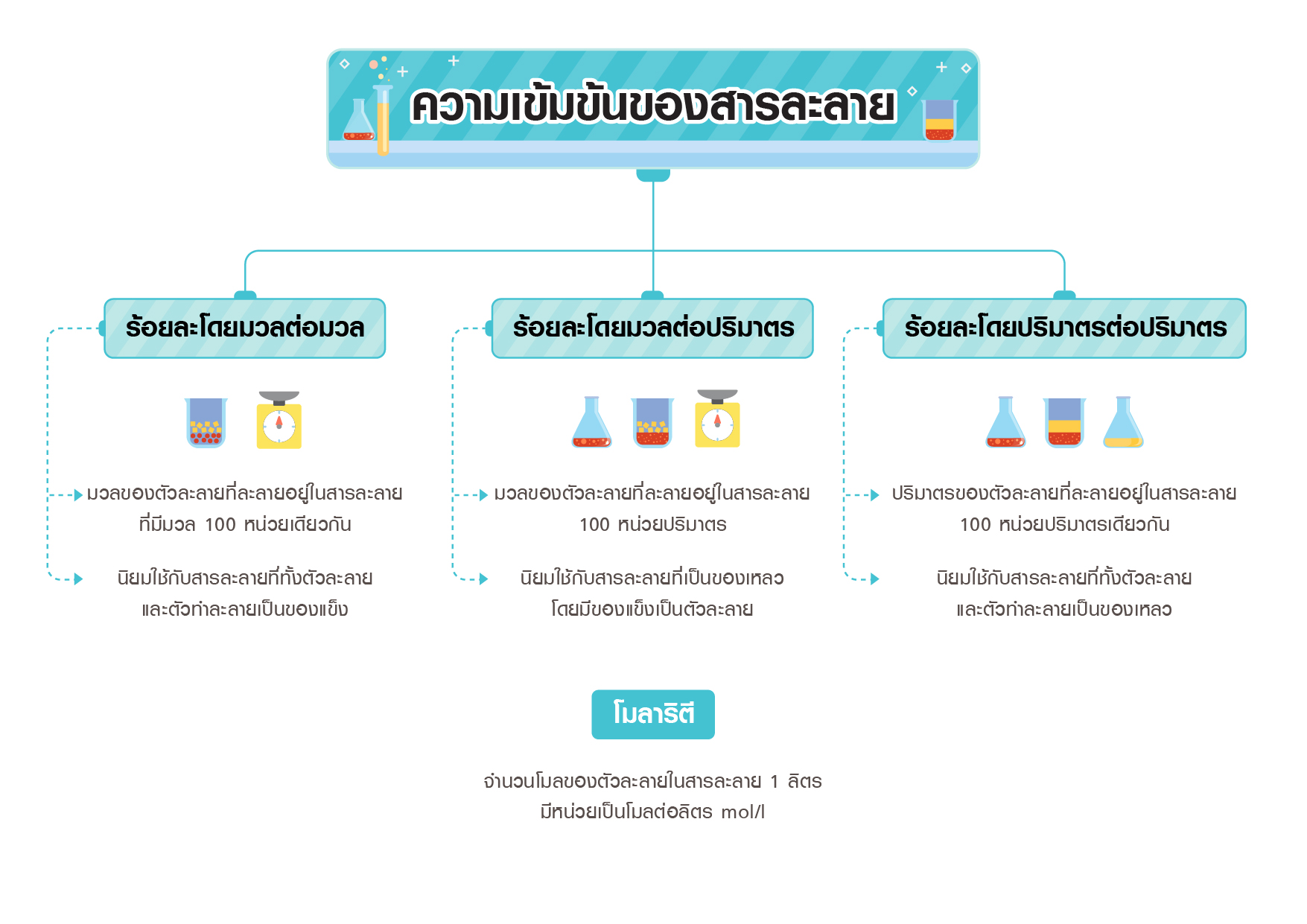
ความเข้มข้นของสารละลาย ความเข้มข้นของสารละลาย ความเข้มข้นของสารละลาย คือ ปริมาณของสารที่เป็นตัวละลายซึ่งละลายอยู่ในสารละลาย 1. ร้อยละ (percent) แบ่งออกเป็นดังนี้ 1) ร้อยละโดยมวล (w/w)บอกถึงมวลของตัวละลายที่ละลายในสารละลาย 100 หน่วยมวล เช่น สารละลายน้ำเชื่อมเข้มข้นร้อยละ 10 โดยมวล คือ ในสารละลายน้ำเชื่อม 100 กรัม ประกอบด้วยน้ำตาล 10 กรัม 2) ร้อยละโดยปริมาตร (v/v)บอกถึงปริมาตรของตัวละลายที่ละลายในสารละลาย 100 หน่วยปริมาตร เช่น สารละลายเอทานอลเข้มข้นร้อยละ 15 โดยปริมาตร คือ ในสารละลาย เอทานอล 100 ลูกบาศก์เซนติเมตร ประกอบด้วยเอทานอล 15 ลูกบาศก์เซนติเมตร 3) ร้อยละโดยมวลต่อปริมาตร (w/v)บอกถึงมวลของตัวละลายในสารละลาย 100 หน่วยปริมาตร เช่น สารละลายเกลือแกง 100 ลูกบาศก์เซนติเมตร ประกอบด้วยเกลือแกง 1 กรัม 2. ส่วนในพันส่วน (part per thousand; ppt) เป็นหน่วยที่บอกมวลของตัวละลายที่มีปริมาณน้อย ละลายในสารละลาย หรือตัวทำละลาย 1 พันส่วน 3. ส่วนในล้านส่วน (part per million; ppm) เป็นหน่วยที่บอกมวลของตัวละลายที่มีปริมาณน้อยมาก ละลายใน สารละลายหรือตัวทำละลาย 1 ล้านส่วน (106 ส่วน) เช่น ปลาตัวหนึ่งมีปรอทปลอมปนอยู่ 0.
Karaoke
2 g ในน้ำ 500 g สารละลายจะมีความเข้มข้นเท่าใดในหน่วยโมลต่อกิโลกรัม 22 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 10 สารละลาย X เข้มข้น 2. 5 m ถ้าในสารละลายนั้นมี X 10 g จงหามวลของน้ำ ในสารละลาย กำหนดให้ X มีมวลโมเลกุลเท่ากับ 250 23 ความเข้มข้นของสารละลาย (5) เศษส่วนโมล ใช้สัญลักษณ์ X เศษส่วนโมลของสารใดในสารละลาย หมายถึง อัตราส่วนจำนวนโมลของสารนั้นกับจำนวนโมลรวมของสารทั้งหมดในสารละลาย เช่น สารละลายชนิดหนึ่งประกอบด้วย สาร A a โมลสาร B b โมล และสาร C c โมล เศษส่วนโมลของ A B และ C เป็นดังนี้ 24 การคำนวณความเข้มข้นของสารละลาย ตัวอย่างที่ 11 จงคำนวณหาเศษส่วนโมลขององค์ประกอบแต่ละชนิดในสารละลายที่ประกอบด้วย สาร A 1. 5 mol สาร B 2. 0 mol และ H2O 5. 0 mol
เป็นการบอกให้เราทราบว่า ตัวทำละลายอยู่กี่ส่วนในสารละลายท้ังหมด 1000 ส่วน ซึ่งไม่ขอนำเสนอรายละเอียดในส่วนนี้ 3. ) เป็นการบอกให้เราทราบว่า ตัวทำละลายอยู่กี่ส่วนในสารละลายท้ังหมด 1, 000, 000 ส่วน ซึ่งไม่ขอนำเสนอรายละเอียดในส่วนนี้
2 ppm หมายความว่า ใน เนื้อปลา 1 ล้านกรัม จะมีปรอทอยู่ 0. 2 กรัม 4. การบอกความเข้มข้น โดยดูจากปริมาณตัวละลายในสารละลาย แบ่งได้เป็นดังนี้ 1) สารละลายเข้มข้นคือ สารละลายที่มีปริมาณตัวละลาย ละลายในสารละลายมาก เมื่อเทียบกับตัวทำละลาย 2) สารละลายเจือจาง คือ สารละลายที่มีปริมาณตัวละลาย ละลายในสารละลายน้อย เมื่อเทียบกับตัวทำละลาย
ความ เข้มข้น ของ สารละลาย pvt. ltd